“Los médicos vamos a seguir trabajando con la industria, simplemente hay que hacerlo de una manera transparente; de lo contrario, puede resultar perjudicial para la investigación, para los oncólogos y para la Medicina en general. Para ello está la declaración de los conflictos de interés, para revelar si existe o no algún vínculo con la industria o con alguna compañía”. Así respondió Monica Morrow, oncóloga jefe de Cirugía de Mama, del departamento de Cirugía del Memorial Sloan Kettering Cancer Center de Nueva York, cuando se le preguntó por el caso Baselga durante su intervención en un encuentro sobre el tratamiento de cáncer de mama celebrado en Madrid y organizado por la farmacéutica Roche.
Entonces, el oncólogo Josep Baselga, no había dimitido de su puesto de director médico del Sloan Kettering Cancer Center de Nueva York, algo que hizo el pasado 13 de septiembre, solo cinco días después de que The New York Times le dedicara parte de su portada, revelando que había recibido importantes cantidades de dinero de la industria farmacéutica -la cifra más repetida en la prensa es de tres millones de euros- sin haberlos declarado ni en los estudios publicados ni en los congresos científicos.
“En todos los ensayos postautorización del medicamento no hay una obligación legal de constatar la financiación, de modo que la obligación es ética”
Pero, ¿tenía que hacerlo o debía hacerlo? Importante matiz. Fernando Abellán, abogado experto en Derecho Sanitario y Bioética y fundador de Derecho Sanitario Asesores, explica que, desde una perspectiva española, “no hay una norma que obligue a hacer estas declaraciones de conflictos de interés a los investigadores de manera general. Está el conocido real decreto de ensayos clínicos con medicamentos que, en su artículo 42.2, obliga a los investigadores a que cuando publiquen el resultado de estos ensayos clínicos declaren el origen del dinero recibido para hacer la investigación” (ver apoyo). Pero el abogado aclara que la investigación no se agota en lo que son los ensayos clínicos con medicamentos, ni tampoco la declaración de conflictos se reduce a dejar por escritor quién ha financiado el proyecto. “En todos los ensayos postautorización del medicamento no hay una obligación legal de constatar la financiación, de modo que la obligación es ética”.

Los códigos éticos de las sociedades científicas y de revistas especializadas recogen como condicionante para publicar los trabajos de investigación, que haya una previa declaración de las relaciones de los autores con la industria.
En este sentido, el abogado destaca que “las sociedades de Cardiología (SEC), Fertilidad (SEF) y Farmacia Familiar y Comunitaria (Sefac), entre otras”, tienen este mandato moral bien recogido en sus códigos. Como buena obligación ética, “su omisión no tiene ningún reproche legal ni administrativo, pero tiene el reproche moral de la comunidad científica”, apostilla.
En su carta de despedida del Sloan, Baselga pedía disculpas a sus colegas por si la situación generada “hubiera causado incomodidad profesional o personal”. Pero la repercusión de la falta de transparencia en la investigación, que se ha puesto de manifiesto este caso, trasciende a los colegas y alcanza a los pacientes. Así lo entiende la excompañera de Baselga en el Sloan, la oncóloga Morrow cuando razona:“No hay ninguna duda de que las relaciones entre la industria y los oncólogos son importantes para investigar sobre fármacos, pero también es muy importante que el público en general sepa que la ciencia tiene una calidad del más alto nivel y que los médicos no estamos pensando en nuestro interés cuando recetamos un tratamiento en concreto”.
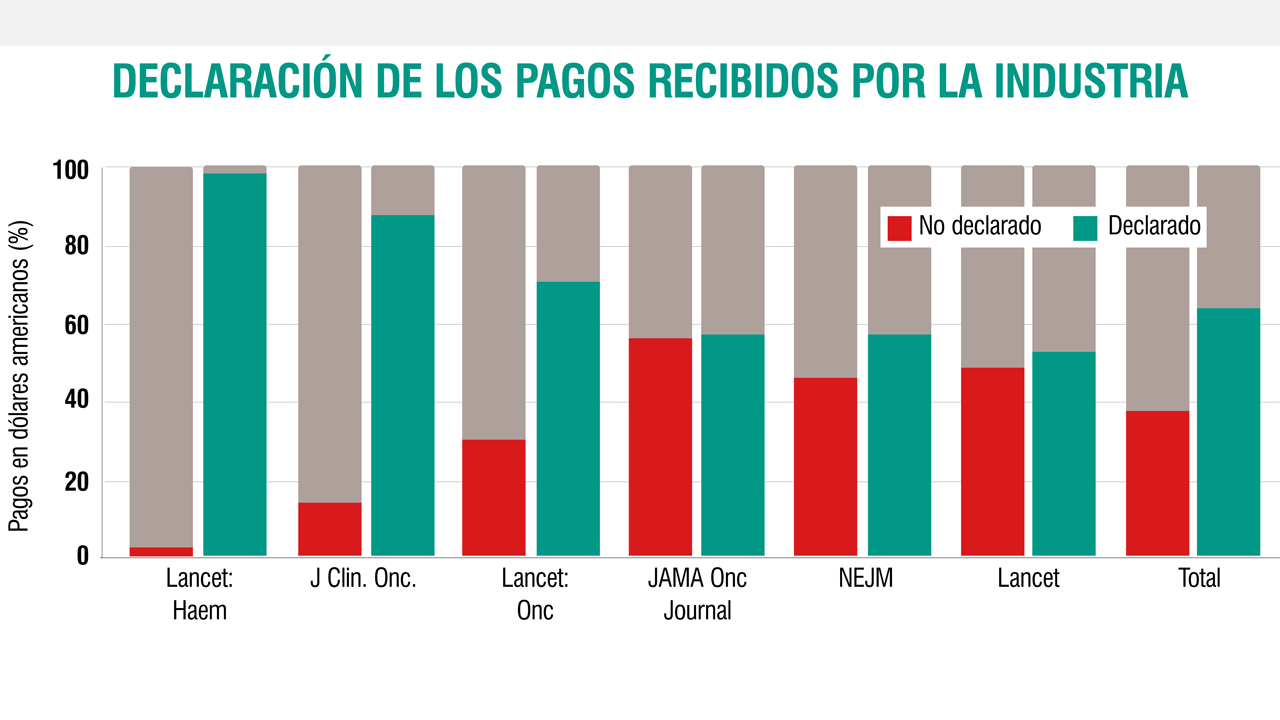
Un estudio publicado en JAMA Oncology, el 30 de agosto de 2018, concluye que un tercio de los investigadores en Oncología no recoge sus conflictos de intereses en sus publicaciones. La muestra ha sido de 344 oncólogos y 43 trabajos publicados en Lancet Haemotology, Journal of Clinical Oncology, Lancet Oncology, JAMA, y The New England Journal of Medicine.
Si algo bueno ha traído este asunto es que ha obligado a las sociedades científicas, a los colegios profesionales y a las revistas científicas a revisar y recordar la necesidad de transparencia en la investigación. Por alusiones, la Sociedad Española de Oncología Médica (SEOM) ha elaborado un documento en respuesta al caso Baselga, recordando que “la investigación de calidad en cáncer en España se rige por un código de ética que incluye la declaración de conflicto de intereses de los investigadores en los artículos publicados en revistas científicas y en la participación de reuniones científicas”.
El mismo día de la dimisión del prestigioso oncólogo catalán, el Colegio de Médicos de Barcelona emitió un comunicado, apuntando que “la transparencia es fundamental, ya que toda la investigación biomédica exige y, a la vez, genera una relación de confianza entre los ciudadanos, los investigadores, las instituciones y la industria”.
“En España un 76 por ciento de los ensayos clínicos en el ámbito del cáncer son patrocinados por la industria, frente al 49 por ciento en Francia, 56 por ciento en Países Bajos, 62 por ciento en Italia y 65 por ciento en Reino Unido”, según el Primer informe sobre la investigación e innovación en cáncer en España, elaborado por la Agencia Española Contra el Cáncer (AECC), la Asociación Española de Investigación sobre el Cáncer (Aseica) y la Fundación La Caixa, y presentado el pasado 11 de septiembre.
Por parte de la industria, la conciencia está muy tranquila (ver apoyo). José Zamarriego, director de la Unidad de Supervisión Deontológica (USD) de Farmaindustria, apunta que el Código ético de esta patronal, además de obligarles a hacer una declaración de todas sus “transferencias de valor”, recomienda “incluir en los contratos con investigadores una cláusula que comprometa al profesional sanitario a declarar que presta servicios de consultoría al laboratorio, cada vez que escriba o se manifieste públicamente respecto de algún asunto objeto de su acuerdo o relacionado con la compañía”.
Sin embargo, hay una importante mayoría que no lo hacen. En un estudio publicado en JAMA Oncology, con fecha de 30 de agosto de este año, se pone de manifiesto que un tercio de los investigadores oncológicos que publican su trabajos en revistas (Lancet, JAMA, The New England Journal of Medicine…) no reflejan el origen de los fondos de su investigación. Así, el caso de Baselga no parece ser una excepción.
El Real Decreto de ensayos clínicos obliga a declarar la financiación en la publicación de estos trabajos
El artículo 42.2 del Real Decreto 1090/2015, de ensayos clínicos con medicamentos, obliga al investigador a que cuando se hagan públicos estudios y trabajos de investigación, dirigidos a la comunidad científica, haga constar “los fondos obtenidos por o para su realización, y la fuente de financiación”. Pero en el cumplimiento de esta norma falta vigilancia. Las inspecciones de Farmacia de las Administraciones autonómicas son las encargadas de velar por este cumplimiento y abrir expedientes en su caso. El abogado Fernando Abellán, no ha conocido ninguna sanción por omitir esta información.
“Para cumplir con la transparencia
en investigación es necesario una ley”
El Código Deontológico de la Organización Médica Colegial recoge la obligación de hacer una declaración de las relaciones con la industria. De su incumplimiento se pueden derivar sanciones, pero nosotros no somos policías y estas prácticas no se denuncian”. Así lo ha puesto de manifiesto Juan José Rodríguez Sendín, presidente de la Comisión Central de Deontología Médica de la OMC.
Sendín se muestra muy duro y crítico con la situación actual, considera que estos conflictos siempre han existido, pero que “ha llegado al momento en que nada justifica la falta de transparencia”. Es contundente al señalar que “hay que declarar todo lo que se recibe de la industria, aunque no todo tiene la misma importancia”.

Para esta batalla por la transparencia, el presidente de la Deontológica considera que no es suficiente con que la declaración del investigador en relación a la industria sea algo voluntario, que figure en los códigos éticos de las revistas científicas o en el código deontológico de la profesión, “hay que dar un paso más y hacerlo obligatorio, solo así se cumplirá”, apostilla.
En este sentido, valora que el caso Baselga haya puesto de manifiesto lo que es “un secreto a voces” y está detrás de muchas críticas a la profesión: “ Es que ciertos médicos son marionetas de la industria”. Además afirmar que “todas las revistas científicas se han puesto en evidencia”.
El artículo 23. 8 del Código Deontológico de la OMC recoge el deber del médico de informar a los colegas y al público en general de sus relaciones con la industria en la investigación o estudios que realicen.y comuniquen
LA INDUSTRIA SE HA AUTOIMPUESTO TRANSPARENCIA
La patronal europea de laboratoriosEfpia acordó en 2013 un código de buenas prácticas con los profesionales sanitarios que ratificó la patronal española Farmaindustria y que obliga a detallar con nombres y apellidos todo pago que haya realizado la industria farmacéutica a profesionales u organizaciones sanitarias. En concreto, es obligatorio detallar identificando con el nombre y apellido al médico u organización receptora todo pago en concepto de ayudas para formación y asistencia a congresos (incluidos los gastos de viaje, comidas y alojamiento) y para prestación de servicios (conferencias, asesorías, etc.). También se identifican el documento que se publica con carácter anual todas las donaciones (que sólo pueden ser a entidades, no a particulares) y los pagos para investigación, que en este caso figuran como una cifra agregada para todo el laboratorio, que no identifica el destino final de esos pagos.
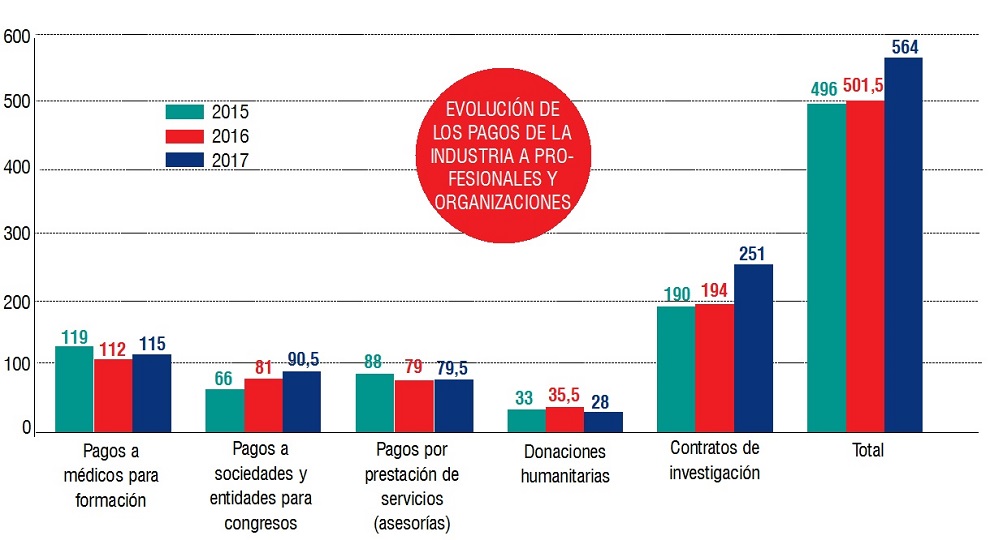
Gracias a este compromiso, cuyos primeros datos se publicaron en junio de 2016, referentes a los datos de 2015 (si bien en ese primer informe aún era voluntaria la identificación con nombres y apellidos, que pasó a ser obligatoria en enero de 2017), se ha podido saber cuánto aporta la industria a los profesionales y organizaciones sanitarias, tratando así de hacer más transparente su relación y posibles conflictos de intereses. Los datos globales publicados en junio de 2018 muestran que en 2017 los laboratorios financiaron 564 millones de euros al sector sanitario, 115 millones en concepto de ayudas a profesionales para asistencia a congresos, 90,3 millones a organizaciones sanitarias (una cifra que no deja de crecer por la tendencia de las sociedades científicas a canalizar las ayudas para formación), 79,5 millones en concepto de prestación de servicios, 28 en donaciones y 251 millones para investigación.
The post El ‘caso Baselga’ recuerda el deber ético de declarar los conflictos de intereses appeared first on Diariomedico.com.
from Diariomedico.com https://ift.tt/2O3Ezzf


